Los resultados muestran que la diversidad bacteriana se volvió relativamente estable una vez que los camarones se desarrollaron a postlarvas

El camarón tigre negro (Penaeus monodon) es una de las especies de camarón de cultivo y comercio más importantes, con una alta demanda y precio en el mercado. Nuestro equipo de investigación ha iniciado recientemente esfuerzos para definir las bacterias intestinales en P. monodon y las interacciones con su huésped, y ya hemos descifrado las diversidades bacterianas de muestras intestinales de camarones de granjas de diferentes ubicaciones que cubren diferentes hábitats y diversas etapas de la vida, desde postlarvas hasta adultos.
Creemos que una mejor comprensión del microbioma [colección de todos los microbios, incluidas bacterias, virus y hongos, que viven naturalmente en los animales y dentro de ellos] de P. monodon allanará el camino para un mejor control de enfermedades y una acuacultura sostenible de la especie. Varios estudios han reportado que la comunidad bacteriana y especies de bacterias individuales pueden desempeñar un papel en la supervivencia de las larvas con respecto a la evaluación de la calidad y el desarrollo de las larvas del camarón, en particular el desarrollo de la inmunidad intestinal. Además, varias aplicaciones de probióticos han mostrado resultados prometedores en la reducción de la mortalidad. Es probable que su modo de acción esté relacionado con la modulación inmunitaria y / o la inhibición antagonista de organismos patógenos.
Para desarrollar prebióticos y probióticos de manera efectiva, es necesario comprender la comunidad de referencia desde las primeras etapas de la vida del camarón. En particular, los camarones recién eclosionados poseen un sistema digestivo inmaduro y estéril antes de que maduren más en las etapas larvarias de nauplio, zoea, mysis y postlarvas. Después de la etapa de nauplio, P. monodon comienza a alimentarse de microalgas o alimentos vivos, lo que permite que las bacterias de fuentes externas comiencen a florecer en el intestino del huésped.
En otros animales, las interacciones entre la inmunidad del huésped y las bacterias no patógenas durante las primeras etapas de la vida son cruciales para el desarrollo posterior de la inmunidad. Se considera que dicha interacción también existe en los camarones porque su sistema inmunológico durante las primeras etapas de la vida en el criadero a menudo todavía se está desarrollando a su máximo potencial. Por lo tanto, las primeras etapas de la vida serán un período privilegiado en el que la aplicación de aditivos alimentarios, como los probióticos, podría ayudar a establecer bacterias intestinales saludables.
Este artículo – adaptado y resumido de la publicación original [Angthong, P. et. al. 2020. Bacterial analysis in the early developmental stages of the black tiger shrimp (Penaeus monodon). Sci Rep 10, 4896 (2020)] – reporta sobre un estudio para caracterizar la comunidad bacteriana de referencia asociada con las etapas tempranas de vida de P. monodon, para respaldar la mejora de la alimentación y el manejo de los criaderos.
Configuración del estudio
Camarones tigre negro fueron criados en el Shrimp Genetic Improvement Center (SGIC, National Science and Technology Development Agency, Surat Thani, Tailandia). Cada familia de camarones se mantuvo en un tanque de fibra de vidrio de 200 litros y se alimentó con dietas basadas en sus etapas de vida. Los estadios de zoea se alimentaron con microalgas (Thalassiosira sp. y Chaetoceros sp.) hasta que alcanzaron el estadio de mysis. Los camarones mysis se alimentaron con artemia y microalgas. Una vez que alcanzaron la etapa postlarval, los camarones fueron alimentados con artemia viva en combinación con alimento comercial.
Se recolectaron muestras de camarón de cada familia (A, B) cuando alcanzaron las etapas de nauplio, zoea, mysis y postlarvas, como se muestra en el diagrama esquemático de la Fig. 1. Debido al pequeño tamaño de las larvas de camarón, se recolectaron muestras agrupadas. Todas las muestras de camarón se lavaron dos veces en agua destilada estéril para minimizar la contaminación arrastrada por el agua de cría.
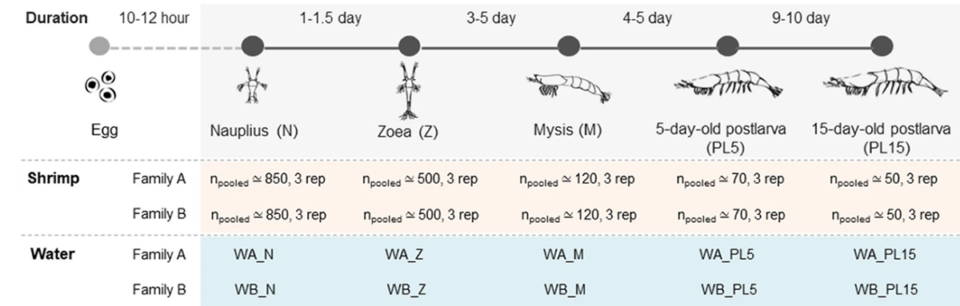
Para obtener información detallada sobre el diseño experimental y la cría de animales; extracción y purificación de ADN; amplificación y secuenciación de genes; cuantificación de la abundancia bacteriana; análisis de la comunidad microbiana y otros análisis realizados, consulte la publicación original.
Resultados y discusión
En años recientes, investigadores han reportado sobre las funciones importantes del microbioma del huésped en la digestión, la mejora del sistema inmunológico y el desarrollo en animales acuáticos, incluido el camarón. Por lo tanto, una de las principales estrategias para lograr una producción sostenible y el control de enfermedades en la cría de animales acuáticos es comprender mejor la relación entre el huésped y la comunidad microbiana.
La caracterización del establecimiento microbiano en sus etapas tempranas de la vida es particularmente crucial debido a sus posibles beneficios para promover un equilibrio microbiano intestinal saludable desde las etapas jóvenes. Nuestro grupo de investigación está involucrado en esfuerzos para investigar la comunidad bacteriana asociada con P. monodon bajo diversas condiciones, y aquí presentamos el primer informe sobre bacterias asociadas con etapas tempranas de vida en P. monodon desde nauplius hasta zoea, mysis y postlarvas.
En este estudio proporcionamos la primera evidencia de microbiota de P. monodon establecida durante las primeras etapas de vida. Identificamos 30 unidades taxonómicas operativas comunes, OTU [una definición operativa utilizada para clasificar grupos de individuos estrechamente relacionados; comúnmente utilizado para categorizar bacterias según la similitud de secuencia] pertenecientes a Proteobacteria, Bacteroidetes y Planctomycetes, lo que sugiere la existencia de establecimiento bacteriano a través del desarrollo de P. monodon desde huevos fertilizados hasta adultos. Estos miembros bacterianos comunes fueron consistentes con reportes anteriores de que se descubrieron Proteobacteria y Bacteroidetes como bacterias autóctonas en camarones juveniles. Sin embargo, las interacciones huésped-bacteria en P. monodon aún requieren una investigación mucho más profunda para obtener una mejor comprensión de sus relaciones y los posibles beneficios para el animal huésped.
También documentamos la asociación de los filos Proteobacteria, Bacteroidetes y Actinobacteria con P. monodon en etapas tempranas de vida. Estos filos dominantes se conocen como microflora típica en varios organismos acuáticos (Fig. 2). Nuestros resultados también mostraron que Vibrio era el género más dominante en todas las etapas del camarón, lo que era consistente con los datos reportados por otros investigadores, y reportado como una bacteria dominante que persiste a través de la metamorfosis del camarón.
Dentro de Bacteroidetes, Tenacibaculum fue el más dominante y se ha reportado que existe mutuamente con las diatomeas planctónicas marinas Chaetoceros sp. y Thalassiosira sp. que fueron alimentadas a camarones en las etapas zoea y mysis en nuestro estudio. Por lo tanto, una mayor abundancia relativa de Tenacibaculum específicamente durante estas dos etapas sugiere que podría ser una población transitoria. Además, se identificó a los Planctomicetos como uno de los filos dominantes durante las primeras etapas de la vida: estas bacterias tienen funciones importantes en los sistemas acuícolas, eliminando compuestos nitrogenados indeseables como el amoníaco y el nitrito.
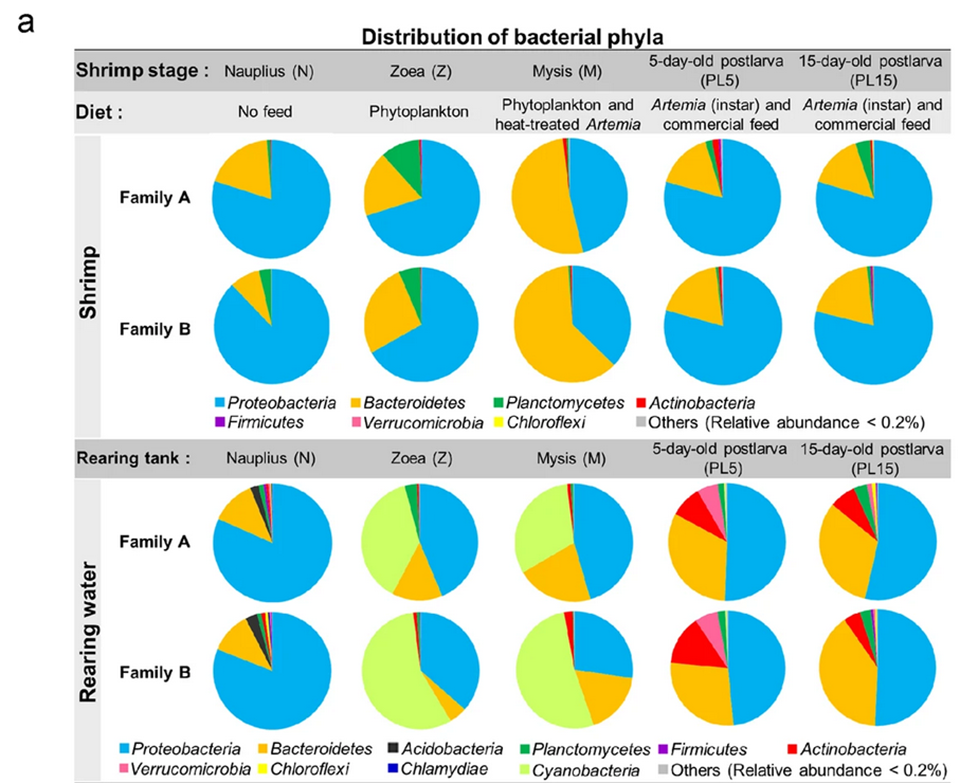
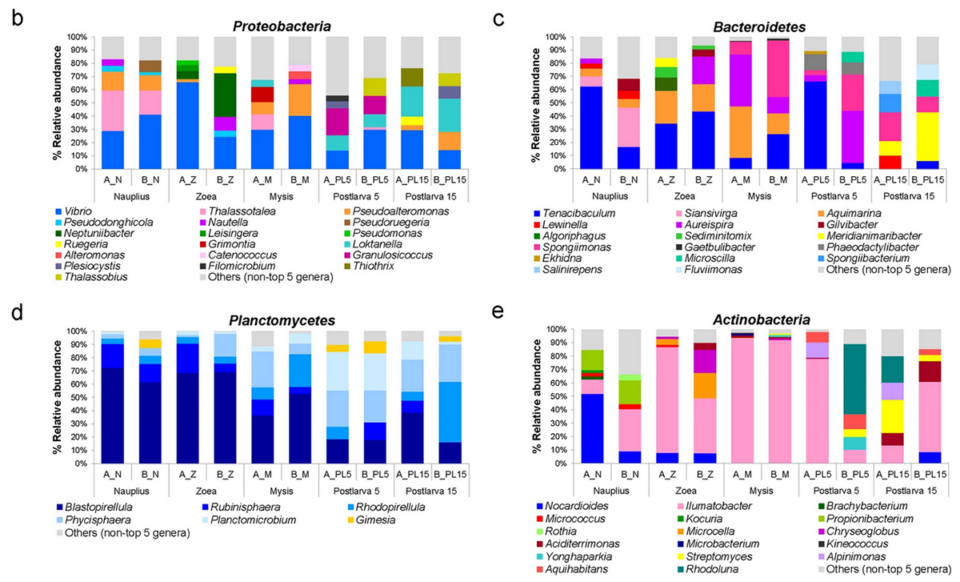
Factores del huésped son responsables del establecimiento de la microbiota en los animales, incluido el camarón. Nuestros resultados mostraron que las etapas de desarrollo fueron un factor importante que afectó la composición de la microbiota. Mientras que las comunidades bacterianas de P. monodon asociadas con la etapa postlarval (postlarvas de 5 y 15 días de edad) fueron similares, las de las etapas anteriores de nauplio, zoea y mysis fueron diferentes. Este cambio drástico en la composición bacteriana podría explicarse por la fisiología del huésped y el cambio en las dietas requeridas en cada etapa. Al igual que otros crustáceos, el camarón sufre una metamorfosis a través de las siguientes etapas: huevo, nauplio, zoea, mysis, postlarva, juvenil y adulto. La progresión del camarón a través de sus etapas de vida también implica la diferencia en su desarrollo fisiológico y los correspondientes requisitos de alimentación.
En nuestro estudio, cuando los huevos de camarón eclosionaron a la primera etapa larvaria (nauplio), se alimentaron de sus reservas durante unos días antes de convertirse en la etapa zoea, donde se alimentaron principalmente con fitoplancton. Los camarones mysis se alimentaron adicionalmente con artemia y fitoplancton tratados térmicamente. Una vez que entraron en la etapa postlarval, sus dietas principales consistieron en artemia viva y gránulos de alimento comercial.
También se han reportado cambios de comunidades bacterianas a lo largo de las etapas de desarrollo en otros invertebrados. Por lo tanto, los cambios en el desarrollo morfológico y fisiológico junto con los ajustes de alimentación durante las primeras etapas de vida podrían tener un impacto en las comunidades bacterianas. Además de las etapas de desarrollo, varios estudios previos han destacado que los antecedentes genéticos de un camarón también pueden influir en su composición bacteriana. En nuestro estudio, observamos consistentemente que los perfiles bacterianos dentro de la misma familia se agruparon juntos en cada etapa de vida, lo que sugiere que la variación genética de diferentes familias de camarones podría ser la base de la diversidad bacteriana observada en la población de camarones, pero el efecto no es tan sustancial como las etapas de desarrollo del hospedador. Nuestros hallazgos fueron consistentes con las conclusiones de otros investigadores que arrojaron luz sobre la relación directa entre las etapas de desarrollo del camarón y el microbioma.
Aparte de los factores del hospedador animal, las condiciones ambientales pueden esencialmente regular la composición del microbioma y se ha demostrado que ejercen una influencia más fuerte en los microbiomas animales que la genética del hospedador. Cada vez hay más evidencia que destaca un fuerte vínculo entre los entornos de cría de camarones (por ejemplo, ubicación, condiciones silvestres, de granja y de laboratorio) y la diversidad microbiana. Nuestro estudio también demostró que los entornos de cría podrían influir considerablemente en la composición bacteriana del camarón P. monodon, así como en sus etapas de desarrollo. Por lo tanto, la modulación microbiana a través del manejo de granja, como la aplicación de probióticos y el acondicionamiento del agua, podría usarse para enriquecer la composición específica del microbioma como un medio factible para desbloquear un mejor rendimiento de crecimiento o resistencia a enfermedades.
Las bacterias comunes podrían ser designadas como candidatas potenciales para el desarrollo de probióticos, ya que son microflora natural que reside dentro del hospedador, lo que permite una administración sostenible y una colonización exitosa en el camarón hospedador. Por ejemplo, Vibrio y Pseudoalteromonas establecidas desde la etapa de nauplio en nuestro estudio se encuentran comúnmente en ambientes acuáticos, y algunas cepas ya han sido reportadas por su valor probiótico contra bacterias patógenas.
Sin embargo, V. alginolyticus, también identificado entre la microbiota compartida por nuestro análisis, ha sido propuesto previamente como un candidato probiótico. Por lo tanto, algunos Vibrio sp. deben utilizarse como probióticos potenciales en el cultivo de camarón con cuidado, ya que algunas especies relacionadas (V. harveyi y V. parahaemolyticus) pueden volverse patógenas en camarones en condiciones desfavorables como altos niveles de materia orgánica, manejo deficiente de la cría o condiciones inmunodeprimidas del huésped. De manera similar, algunas especies de Pseudoalteromonas son motivo de preocupación como bacterias patógenas, mientras que otras se han utilizado como probióticos en varios organismos marinos, incluido el camarón azul (L. stylirostris).
Sin embargo, serán necesarias más comparaciones de la microbiota asociada con las etapas tempranas de vida de P. monodon de diferentes granjas camaroneras para caracterizar el microbioma central compartido por esta especie de camarón.
Perspectivas
Nuestros resultados demostraron que las comunidades bacterianas asociadas con P. monodon durante las primeras etapas de vida del camarón podrían ser moduladas por etapas de vida a través de las diferencias fisiológicas y las dietas del hospedador. Nuestros hallazgos ofrecen los primeros conocimientos sobre el establecimiento y el ensamblaje bacteriano en las primeras etapas de la vida de P. monodon, donde el entorno de cría juega un papel mínimo en la influencia de la microbiota del camarón. Este conocimiento fundamental apoyará el desarrollo sostenible de probióticos o aditivos alimentarios para la acuacultura que contribuirán a mejorar las tasas de supervivencia y la absorción de nutrientes en el cultivo de P. monodon.
Será necesaria una investigación futura adicional sobre las interacciones huésped-microbiota para comprender completamente la dinámica de las comunidades bacterianas en las diferentes etapas de la vida y cómo desempeñan un papel en el bienestar de esta especie de camarón.
Ahora que Ud. ha terminado de leer este artículo...
… esperamos que considere apoyar nuestra misión de documentar la evolución de la industria acuícola mundial y compartir el conocimiento expansivo de nuestra amplia red de colaboradores cada semana.
Al convertirse en miembro de la Global Seafood Alliance, se asegura de que todo el trabajo pre-competitivo que realizamos a través de beneficios, recursos y eventos para miembros pueda continuar. La membresía individual cuesta solo $50 al año. Los miembros individuales y corporativos de la GSA reciben acceso gratuito a una serie de eventos virtuales GOAL a partir de Abril. Únase ahora.
¿No es miembro de la GSA? Únase a nosotros.
Authors
-
Pacharaporn Angthong, Ph.D.
Microarray Research Team, National Center for Genetic Engineering and Biotechnology, 113 Thailand Science Park, Phahonyothin Road, Khlong Luang, Pathum Thani, 12120, Thailand
-
Tanaporn Uengwetwanit, Ph.D.
Microarray Research Team, National Center for Genetic Engineering and Biotechnology, 113 Thailand Science Park, Phahonyothin Road, Khlong Luang, Pathum Thani, 12120, Thailand
-
Sopacha Arayamethakorn, M.S.
Microarray Research Team, National Center for Genetic Engineering and Biotechnology, 113 Thailand Science Park, Phahonyothin Road, Khlong Luang, Pathum Thani, 12120, Thailand
-
Panomkorn Chaitongsakul
Shrimp Genetic Improvement Center (SGIC), National Center for Genetic Engineering and Biotechnology, Surat Thani, 84110, Thailand
-
Nitsara Karoonuthaisiri, Ph.D.
Microarray Research Team, National Center for Genetic Engineering and Biotechnology, 113 Thailand Science Park, Phahonyothin Road, Khlong Luang, Pathum Thani, 12120, Thailand
-
Wanilada Rungrassamee, Ph.D.
Corresponding author
Microarray Research Team, National Center for Genetic Engineering and Biotechnology, 113 Thailand Science Park, Phahonyothin Road, Khlong Luang, Pathum Thani, 12120, Thailand
Tagged With
Related Posts

Health & Welfare
Caracterización de comunidades bacterianas en el agua, intestino del camarón azul del Pacífico
Este estudio proporciona información sobre la comunidad bacteriana asociada con biofloc y su influencia en la microbiota intestinal del camarón azul del Pacífico.

Health & Welfare
Bacterioma intestinal de camarones blancos del Pacífico en sistemas de biofloc y de agua clara
Descripción global del bacterioma intestinal del camarón blanco del Pacífico en sistemas de biofloc y de agua clara, y después de un desafío oral por el virus del síndrome de la mancha blanca.

Health & Welfare
El parámetro de calidad del agua a menudo ignorado: pH
La atención al pH, una escala numérica usada para especificar la condición ácida o alcalina de una solución acuosa, es muy importante. La reducción de la biomasa y de las tasas de alimentación junto con el control del fitoplancton y el encalado pueden mantener el pH en valores deseables.

Responsibility
Relaciones carbono-nitrógeno en fertilización de estanques y sistemas de biofloc
El Prof. Claude Boyd discute la importancia de las relaciones carbono-nitrógeno para la fertilización de estanques y los sistemas biofloc, y la relevancia de las aportaciones precisas de carbohidratos.



