Determinación de la capacidad anti-inflamatoria e inmunogénica in vitro

El uso de harina de insectos, principalmente derivada de larvas de mosca soldado negra (BSF, Hermetia illucens) como ingrediente de alimentos acuícolas está bajo investigación, mientras que la industria de alimentos acuícolas lo adopta cada vez más. La mayoría de las investigaciones se han centrado en el potencial de la harina de insectos como ingrediente proteico alternativo para varias especies de peces – como la trucha arcoíris, el salmón, la carpa, la lubina y el bagre – mientras que solo unos pocos estudios han investigado los beneficios inmunológicos de la harina de insectos.
Aquí presentamos los resultados de un proyecto destinado a investigar la capacidad inmunogénica (o pro-inflamatoria) y anti-inflamatoria in vitro de la harina de mosca soldado negra BSF orgánica en comparación con otros ingredientes disponibles comercialmente.
Configuración del estudio
Ingredientes evaluados
Las descripciones de los ingredientes investigados a lo largo de este proyecto se incluyen en la Tabla 1. Todas las muestras se disolvieron en agua, se mezclaron a temperatura ambiente durante una hora y se centrifugaron para separar el material soluble (sobrenadante) del insoluble (gránulos). El sobrenadante, que contenía componentes solubles, se filtró a 0,22 µm y se almacenó a -20 grados-C hasta que se necesitó para los ensayos celulares.
Rombenso, BSF, Tabla 1
| Ingredientes evaluados | Abreviaciones | Concentraciones evaluadas |
|---|
Ingredientes evaluados | Abreviaciones | Concentraciones evaluadas |
|---|---|---|
| Harina orgánica de insectos, mosca soldado negro entera | BSF Pre | 20 mg/mL |
| Harina de insecto orgánica de mosca soldado negra prensada por expulsor, baja en grasa | BST Post | 20 mg/mL |
| Harina de pescado | – | 20 mg/mL |
| Polvo de grillo | – | 20 mg/mL |
| Quercetina | – | 100 µM |
Ensayos basados en células
La línea celular de macrófagos de ratón RAW264.7 se cultivó in vitro para producir óxido nítrico (NO), una molécula de señalización que juega un papel vital en la patogénesis de la inflamación. La estimulación de la producción de NO representa respuestas inmunogénicas o pro-inflamatorias, mientras que la disminución de la producción de NO sugiere actividad anti-inflamatoria. Se cultivaron células de macrófagos de ratón RAW264.7 para producir dos ensayos basados en células diferentes.
Capacidad inmunogénica (pro-inflamatoria) in vitro

Para estimular la producción de NO y observar cualquier respuesta inmunogénica (o pro-inflamatoria), las células se trataron con lipopolisacárido bacteriano (LPS) o los ingredientes de prueba. Para garantizar que ningún efecto del tratamiento estuviera relacionado con la toxicidad (que podría dar lugar a falsos positivos), se midió la viabilidad celular en el ensayo en respuesta a todas las muestras del proyecto y osciló entre el 106 y el 124 por ciento (expresado como porcentaje en comparación con las células no tratadas) .
Se siguió la siguiente metodología:
- Se cultivaron 7 células en matraces y se mantuvieron a 37 grados-C con 5 por ciento de CO2 en medio de crecimiento (DMEM, 10 por ciento de suero bovino fetal).
- Las células se cultivaron hasta aproximadamente un 90 por ciento de confluencia antes de recolectarlas y contarlas.
- Se sembraron 6×105 células/ml en placas transparentes de 96 pocillos y se cultivaron durante dos días en presencia de extractos acuosos preparados a partir de muestras de prueba (consulte la Tabla 1) diluidos en medios de cultivo.
- Después de dos días, los medios de cultivo celular se transfirieron a placas negras de 96 pocillos para la producción de nitrito (es decir, detección de óxido nítrico) utilizando DAN (2,3-diaminonaftalina).
- Después de 10 minutos, se midió la fluorescencia (Ex 360 nm; Em 430 nm) y se representó frente a una curva estándar de nitrito.
- Los resultados se extrapolaron aún más utilizando una curva estándar de producción de LPS-nitrito.
- Las células que quedaban en las placas transparentes se lavaron antes de medir la viabilidad celular a 490 nm, utilizando el Ensayo de Proliferación Celular de una Solución Acuosa CellTiter96 (Promega).
Capacidad anti-inflamatoria in vitro
En este ensayo, las células se co-trataron con LPS (para inducir la producción de NO) y una muestra de prueba para determinar si alguna muestra podía inhibir la producción de NO en consonancia con la actividad anti-inflamatoria. La actividad anti-inflamatoria se comparó con la acción de la quercetina pura, un fitosterol de origen vegetal y un conocido compuesto anti-inflamatorio. Una vez más, para garantizar que ningún efecto del tratamiento estuviera relacionado con la toxicidad, se midió la viabilidad celular en el ensayo en respuesta a todas las muestras del proyecto y osciló entre el 70 y el 85 por ciento (expresado como porcentaje en comparación con las células no tratadas).
Se siguió la siguiente metodología:
- Se cultivaron 7 células en matraces y se mantuvieron a 37 grados-C con 5 por ciento de CO2 en medio de crecimiento (DMEM, 10 por ciento de suero bovino fetal).
- Las células se cultivaron hasta aproximadamente un 90 por ciento de confluencia antes de recolectarlas y contarlas.
- Se sembraron 6×105 células/ml en placas transparentes de 96 pocillos y se cultivaron durante 2 días en presencia de extractos de agua preparados a partir de muestras del proyecto (consulte la Tabla 1) y LPS diluido en medios de crecimiento.
- Después de dos días, los medios de cultivo celular se transfirieron a placas negras de 96 pocillos para la producción de nitrito (es decir, detección de óxido nítrico) utilizando DAN (2,3-diaminonaftalina).
- Después de 10 minutos, se midió la fluorescencia (Ex 360 nm; Em 430 nm) y se representó frente a una curva estándar de nitrito.
- Los resultados se extrapolaron aún más utilizando una curva estándar de producción de LPS-nitrito y se compararon con una respuesta a la dosis de quercetina.
- Las células que quedaban en las placas transparentes se lavaron antes de medir la viabilidad celular a 490 nm utilizando el ensayo de proliferación celular de una solución acuosa CellTiter96 (Promega).
Análisis estadísticos
Los resultados se analizaron en busca de diferencias significativas mediante el análisis de varianza uni-direccional (ANOVA) seguido de la prueba de comparación múltiple de Tukey o Dunnett. Antes de los análisis, los supuestos de ANOVA de normalidad de los residuos y homogeneidad de las varianzas se probaron utilizando las pruebas de Shapiro-Wilk y Levene, respectivamente. Las diferencias se consideraron significativas cuando P <0,05. Todos los análisis estadísticos se realizaron con el software GraphPad Prism 9.
Composición química de los ingredientes de prueba

Todos los ingredientes de los alimentos acuícolas de prueba, excepto el polvo de grillo comercial, fueron analizados por el personal de CSIRO utilizando métodos establecidos de mejores prácticas en el Laboratorio Analítico del Precinto de Biociencia de Queensland. La composición del polvo de grillo fue proporcionada por el proveedor. Los análisis se basaron en la Asociación de Químicos Agrícolas Oficiales (AOAC, 2016).
El contenido de materia seca se determinó mediante análisis gravimétrico después de secar a 105 grados-C durante 16 horas. El contenido de cenizas se determinó en base al cambio de masa después de la combustión en un horno de mufla (1521CAF Ashing Furnace, S.E.M Equipment, Australia) a 550 grados-C durante 16 horas. La porción de lípidos totales se extrajo según el método propuesto por Folch et al. (1957) y se utilizó para determinar el contenido de lípidos crudos. La medición del contenido de nitrógeno (N) total se realizó con un analizador elemental orgánico CHNS/O (Thermo Fisher Scientific, Waltham, Mass., EE. UU.) y se usó para calcular el contenido de proteína cruda de la muestra en función de N x 6,25. El contenido de carbohidratos se calculó por diferencia. La composición química de las diversas muestras se muestra en la Tabla 2.
Resultados y discusión
Según los hallazgos in vitro de este estudio, las larvas de BSF contienen moléculas inmunogénicas, con el potencial de modular la inmunidad in vivo, y moléculas anti-inflamatorias que pueden aliviar las respuestas inflamatorias in vivo. Los hallazgos de este proyecto muestran que los productos orgánicos de BSF pueden usarse como un aditivo alimentario funcional para alimentos acuícolas, y que refinar la composición química de los productos orgánicos de BSF podría mejorar su valor como fuente de proteína alternativa, dependiendo de las especies acuícolas objetivo.
Capacidad inmunogénica (o pro-inflamatoria) in vitro
La capacidad inmunogénica (o pro-inflamatoria) (expresada como equivalentes de LPS ng por gramo de material de partida) se muestra en la Fig. 1 y fue significativamente mayor en las muestras BSF Pre y Post en comparación con otros ingredientes de prueba. Además, BSF Post exhibió una capacidad inmunogénica significativamente mayor en comparación con BSF Pre.
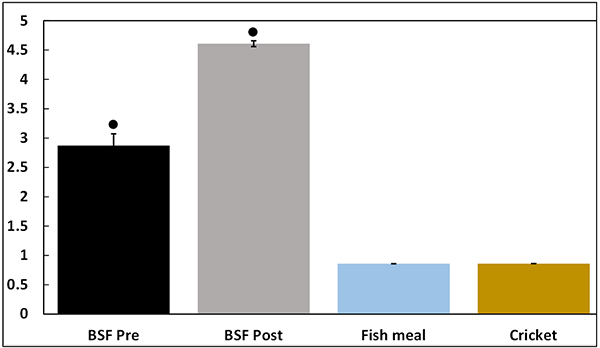
* Indica diferencias significativas en comparación con el polvo de grillo mediante un análisis de varianza de una vía seguido de la prueba de comparación múltiple de Tukey.
Recientes estudios in vivo han explorado la capacidad inmunogénica de complementar la alimentación animal con larvas de BSF (referencias disponibles del autor correspondiente) y han observado impactos positivos en el crecimiento, la salud intestinal y la respuesta inmunitaria. Recientes estudios in vitro también han explorado la capacidad inmunogénica de las larvas de BSF. Por ejemplo, Ali y sus colaboradores exploraron la producción de NO por células RAW264.7 en respuesta a extractos de larvas de BSF y un nuevo polisacárido bioactivo (denominado dipterosa-BSF) purificado a partir de extractos de larvas de BSF. La dipterosa-BSF incluso estimuló la producción de NO de manera similar a LPS. Por lo tanto, estos hallazgos publicados respaldan los resultados del presente estudio y sugieren que las harinas o extractos preparados a partir de larvas de BSF pueden mejorar la salud animal a través de la inmunomodulación cuando se incluyen en la dieta.
En el presente estudio, BSF Pre y BSF Post exhibieron una mayor actividad inmunogénica que el polvo de grillo y la harina de pescado. Además, BSF Post aumentó significativamente más la producción de NO que BSF Pre, lo que sugiere que el prensado por expulsor puede mejorar la capacidad inmunogénica de BSF. Esto puede deberse al enriquecimiento de moléculas inmunogénicas o a la mejora de la solubilidad después del prensado por expulsor. El procesamiento adicional puede mejorar aún más la capacidad inmunogénica de BSF Post. Aunque se podría especular que la propiedad pro-inflamatoria de BSF puede hacer que las altas tasas de inclusión sean menos deseables, particularmente si el sistema inmunológico está demasiado estimulado, aunque la literatura actual sugiere que no hay deficiencias en este contexto (como se describe a continuación).
Capacidad anti-inflamatoria in vitro
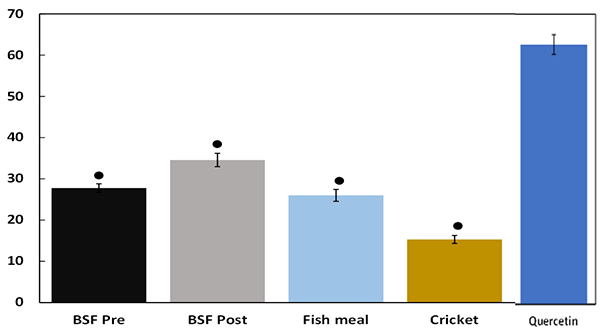
La capacidad anti-inflamatoria (expresada como porcentaje de inhibición de la producción de NO) se muestra en la Fig. 2 y fue similar en respuesta a muestras de harina de pescado y BSF Pre, BSF Post. En comparación con el tratamiento celular con quercetina (una molécula anti-inflamatoria de origen vegetal), la capacidad anti-inflamatoria fue significativamente menor en respuesta a BSF Pre, BSF Post, harina de pescado y polvo de grillo. Sin embargo, las muestras BSF Pre y BSF Post exhibieron una actividad anti-inflamatoria significativamente mayor en comparación con el polvo de grillo.
Un estudio in vivo reciente exploró el impacto de la suplementación de alimentos acuícolas con BSF en la trucha arcoíris y reveló evidencia de disminución de la inflamación intestinal, particularmente cuando se complementa con dietas a base de soya que se sabe que inducen inflamación y reducen la integridad de la barrera intestinal. En el estudio actual, la capacidad anti-inflamatoria fue similar en respuesta a BSF Pre, BSF Post y muestras de harina de pescado y significativamente menor que la respuesta celular a la quercetina. Sin embargo, las muestras BSF Pre y BSF Post exhibieron una actividad anti=inflamatoria significativamente mayor en comparación con el polvo de grillo.
Composición química
La composición química de las harinas de BSF orgánicas las convierte en ingredientes deseables para alimentos acuícolas y se encuentra dentro del rango informado en la literatura. Esos productos son ricos en proteínas y contienen niveles relativamente bajos de cenizas y carbohidratos en comparación con otras fuentes de proteínas alternativas. Se debe considerar la reducción del contenido de lípidos de las harinas BSF para ayudar a lograr un mejor valor nutricional para el mercado de alimentos acuícolas (por ejemplo, niveles de lípidos entre 5 y 12 por ciento, según las especies acuícolas objetivo). Los niveles más bajos de lípidos en las harinas de BSF aumentarán, en consecuencia, el contenido de proteínas y carbohidratos y probablemente aumentarán la capacidad inmunogénica y anti-inflamatoria, como se analiza a continuación.
Rombenso, BSF, Tabla 2
| Medida de composición | BSF Pre | BSF Post | Harina de pescado | Polvo de grillo comercial* |
|---|
Medida de composición | BSF Pre | BSF Post | Harina de pescado | Polvo de grillo comercial* |
|---|---|---|---|---|
| Materia seca (%) | 86.4 | 87.9 | 87.3 | – |
| Ceniza (%) | 9.2 | 10.2 | 15.3 | – |
| Lípidos totales (%) | 21 | 14.7 | 10.6 | 9.5 |
| Proteína total (%) | 45.8 | 50.4 | 72.9 | 68.5 |
| Carbohidratos (%) | 10.2 | 12.5 | 1.2 | 1 |
* Composición de la muestra suministrada con la muestra.
Consideraciones finales
La harina de insectos BSF orgánica contiene moléculas inmunogénicas que fueron proinflamatorias e indujeron una producción de NO significativamente mayor que la harina de pescado y el polvo de grillo. En particular, el prensado por expulsor mejoró significativamente la capacidad inmunogénica de la harina de insectos BSF orgánica en un 60 por ciento. Las harinas orgánicas BSF parecen ser adecuadas como ingredientes y pueden tener propiedades funcionales de relevancia estratégica para los alimentos acuícolas. Se recomienda optimizar la composición de las harinas, en particular mediante el desgrasado para aumentar el contenido de proteínas, a fin de refinar este producto para las necesidades nutricionales de las especies acuícolas carnívoras.
Más estudios in vitro podrían explorar diferentes técnicas de procesamiento y examinar las diferentes fracciones de macronutrientes que mejoran el potencial inmunogénico de la harina de insectos BSF orgánica. También se podrían considerar estudios en animales para investigar el potencial de la harina de insectos BSF orgánica en diferentes tasas de inclusión (aditivo funcional <10 por ciento; fuente de proteína 10-40 por ciento) para mejorar la salud intestinal, reducir la gravedad de las enfermedades bacterianas/virales y ser utilizada como una fuente de proteína alternativa comercialmente rentable.
Referencias disponibles del autor correspondiente.
Ahora que Ud. ha terminado de leer este artículo...
… esperamos que considere apoyar nuestra misión de documentar la evolución de la industria acuícola mundial y compartir el conocimiento expansivo de nuestra amplia red de colaboradores cada semana.
Al convertirse en miembro de la Global Seafood Alliance, se asegura de que todo el trabajo pre-competitivo que realizamos a través de beneficios, recursos y eventos para miembros pueda continuar. La membresía individual cuesta solo $50 al año.
¿No es miembro de la GSA? Únase a nosotros.
Authors
-

Artur Rombenso, Ph.D.
Corresponding author
Senior Research Scientist – Animal Nutrition
CSIRO Livestock & Aquaculture Program
Bribie Island Research Centre, 144 North St, Woorim, QLD 4507 AUS -
Anca Rusu
Research Technician – Molecular Nutrition
CSIRO Livestock & Aquaculture Program
Queensland Bioscience Precinct, 306 Carmody Road, St Lucia, QLD 4067 AUS -
Andrew Porter
CEO
BSF Organic Pty. Ltd
1485 Ballan Road, Anakie, VIC, 3213 -
Nicholas Bourne
Research Technician – Animal Nutrition
CSIRO Livestock & Aquaculture Program
Queensland Bioscience Precinct, 306 Carmody Road, St Lucia, QLD 4067 AUS -
Ha Truong, Ph.D.
Research Scientist – Animal Nutrition
CSIRO Livestock & Aquaculture Program
Bribie Island Research Centre, 144 North St, Woorim, QLD 4507 AUS -
Cedric Simon, Ph.D.
Principal Research Scientist – Animal Nutrition
CSIRO Livestock & Aquaculture Program
Queensland Bioscience Precinct, 306 Carmody Road, St Lucia, QLD 4067 AUS -
Simone Osborne, Ph.D.
Senior Research Scientist – Molecular Nutrition
CSIRO Livestock & Aquaculture Program
Queensland Bioscience Precinct, 306 Carmody Road, St. Lucia, QLD 4067 AUS
Tagged With
Related Posts

Health & Welfare
Evaluación dietética de la harina de larvas de mosca soldado negra sobre el crecimiento y la salud del camarón blanco del Pacífico
La inclusión de harina de larvas de mosca soldado negra, para reemplazar la harina de pescado en las dietas de L. vannamei, mejora la salud del camarón y su resistencia a enfermedades.

Aquafeeds
Gente de moscas: Canadá abre la puerta a las compañías de alimentos a base de insectos
La película de ciencia ficción "The Fly" advirtió sobre la combinación de moscas y tecnología, pero los granjeros de moscas soldado negro de alta tecnología están aprovechando una oportunidad real en la acuacultura.

Aquafeeds
La soya ayudó a convertir la acuacultura en una fuerza global. ¿Hasta dónde la puede llevar?
La soya ha impulsado el crecimiento de la acuacultura, pero las preocupaciones ambientales y sociales de algunas áreas productoras están instigando a algunos acuacultores a evaluar la situación.

Aquafeeds
Evaluación del reemplazo dietético del aceite de pescado en el pámpano juvenil de Florida
El estudio evaluó el rendimiento de producción y la composición de tejidos de pámpano juvenil de Florida alimentado con dietas que contenían aceite de pescado o mezclas 25:75 de aceite de pescado y varias otras fuentes de lípidos.



